影像醫學部 李威興醫師撰稿
陳名聖醫師校閱編修
調查發現,約有五成七民眾認為自己或爸媽失智是件丟臉的事,也由於恐懼,造成了失智症的篩檢阻礙,延誤早期發現及治療的機會。
據統計,台灣65歲以上的老人每12人即有1位失智,而80歲以上的老人則每5人即有1位是失智者,阿茲海默症最大的風險因子即是年齡的增長。隨國人平均壽命增長及人口結構老化,台灣失智症協會預測,民國150年失智人口估計將逾85萬人,代表著每100位台灣人就有近5位是失智者(表一),如此高的佔比,提醒著我們深入了解失智症並及早預防的重要性。
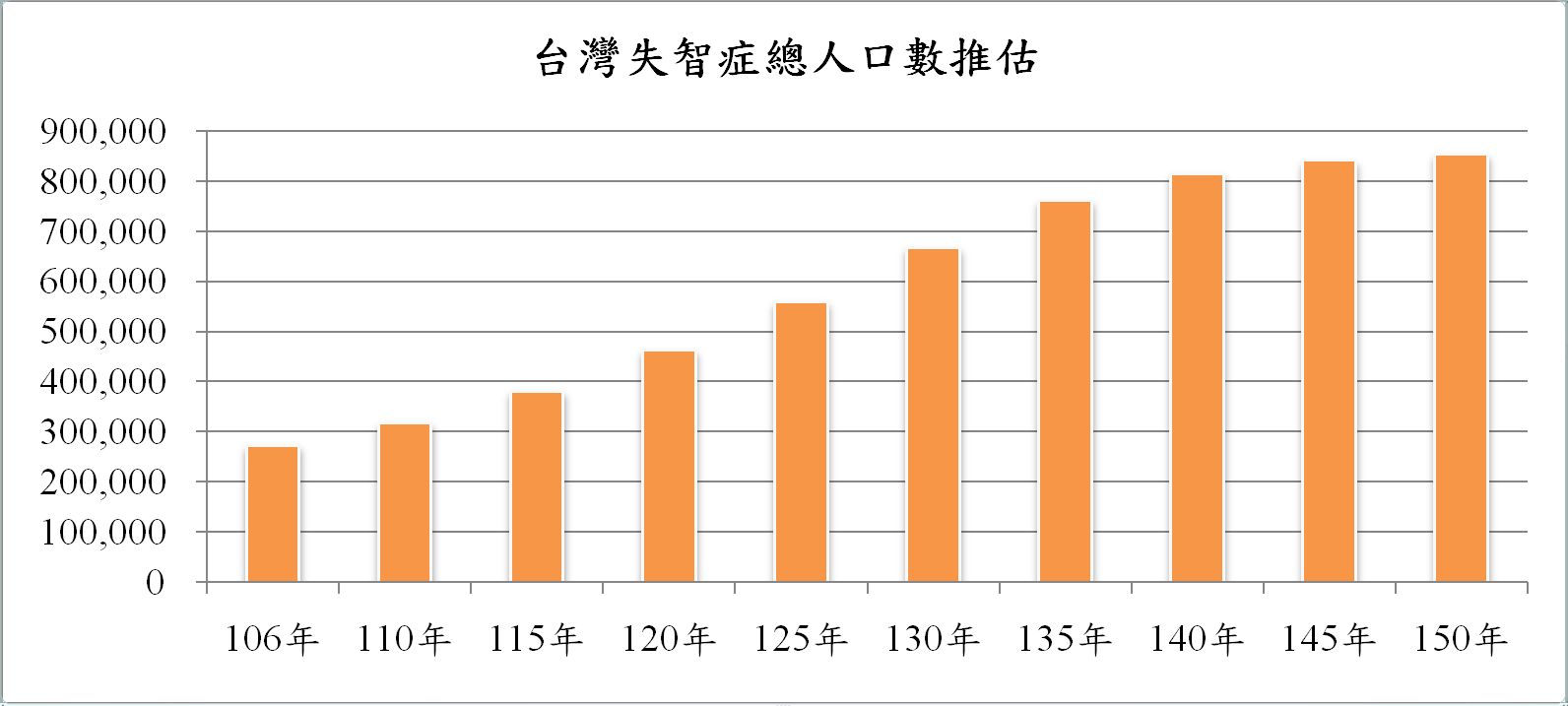
(表一)台灣失智症總人口數推估。│資料來源:台灣失智症協會
▎失智症的種類
失智症並不屬於正常的老化現象,而是一種大腦疾病。其症狀不僅是記憶力減退,還會影響其他認知功能,包括語言、空間感、計算力、判斷力、抽象思考、注意力等各方面的功能退化,嚴重程度足以干擾日常生活。
失智症主要分為退化性失智症、血管性失智症及其他原因產生的認知功能障礙(圖一)。其中以阿茲海默症(Alzheimer disease)最常見,約佔失智症病例的60%,俗稱老年失智症或老年癡呆症,是一種大腦不可逆、進行性的神經退化性疾病。
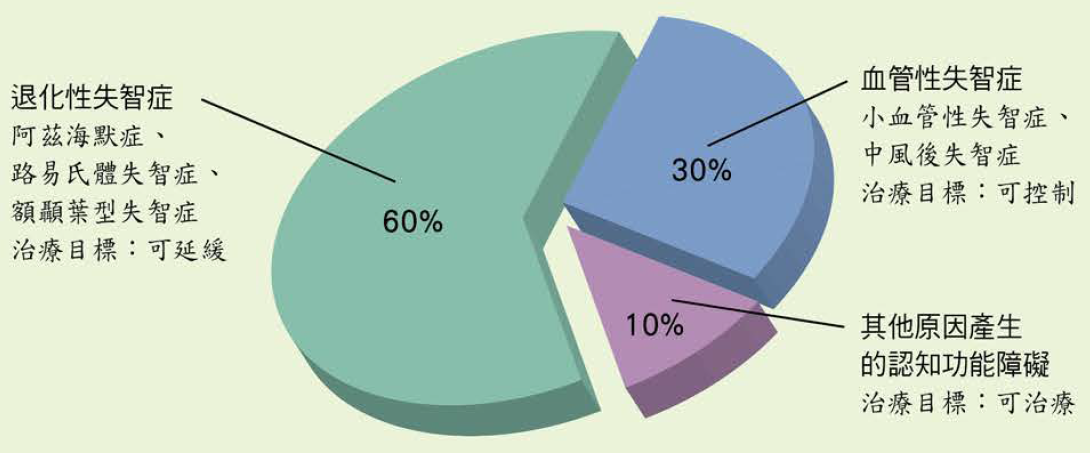
(圖一)失智症的種類
而第二種常見病因為血管性失智症,約佔30%,近期發現阿茲海默症和血管性失智症之間有重疊並存情形,又稱為混合型,而小血管疾病(圖二)可能同時是導致失智症的促進因子和病因。其他不太常見但同屬於退化性失智症,且同樣具破壞性認知功能障礙的神經退化性疾病是:路易氏體失智症 (Lewy body dementia) 約佔4.2%、額顳葉型失智症 (frontotemporal dementia)約佔2%(圖三)。
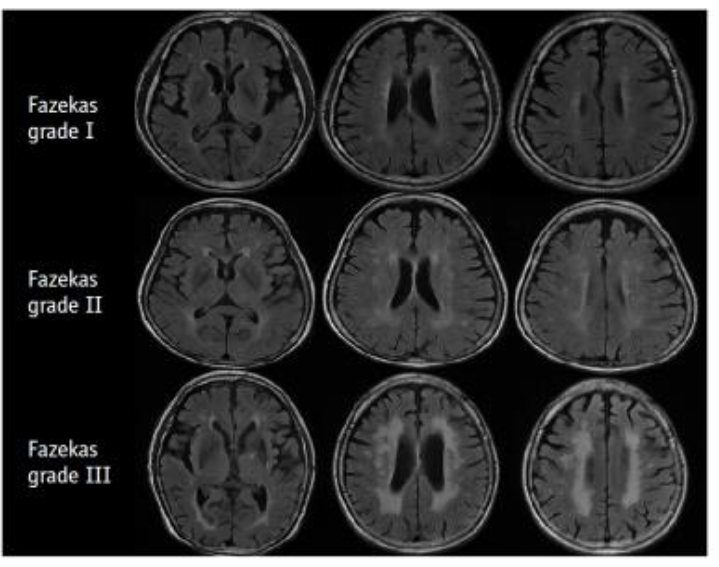
( 圖二)血管性失智症之小血管缺血病變白質斑塊分級。│AJR 1987;149:351-356

(圖三)額顳葉型失智症腦部影像。│Osborn’s brain imaging, pathology, and anatomy 2013 1st edition, p 973 Korean J Radiol 17(6), Nov/Dec 2016
還有許多疾病,例如營養失調(如缺乏維他命B12、葉酸等)、藥物副作用、酗酒、睡眠障礙、甲狀腺功能低下、中樞神經系統感染(如梅毒、愛滋病等)、憂鬱症和焦慮等都會影響認知功能,但這些都是可治療的。此外,常壓性水腦症、腦部腫瘤、腦部創傷、腦出血(硬腦膜下血腫)和中風患者也可能發生認知功能障礙。
失智症目前採取預防勝於治療的方式,應透過早期診斷,確診失智症類型,才不會延誤治療時機。以佔最大宗的阿茲海默症為例,雖然目前無法根治,但可經由藥物來改善臨床症狀並延緩病程,若能早期發現則延緩退化的效果越好。這也是醫學界想盡辦法突破檢驗技術的原因,若能在認知功能正常的阿茲海默症臨床前期,將罹病風險檢測出來,就能儘早延緩病程惡化。
▎阿茲海默症的病徵及病程
阿茲海默症早期病徵最明顯為記憶力衰退,患者對時間、地點和人物的辨認,會有兩種以上的認知功能障礙。慢慢地會發展到其他認知功能也受到影響,終至日常生活不能再自理。當患者達到失智的程度時,醫師會根據臨床表現為典型或非典型,給予很可能(probable)或者有可能(possible)是阿茲海默症的臨床診斷。
阿茲海默症的病程又分為臨床前期(潛伏期長,約15至20年)、前驅期及明顯阿茲海默症(病程緩慢進展約8至10年),整個病程約進行20至30年。
● 臨床前期preclinical:認知功能正常,但生物標記已有變化。
● 前驅期prodromal:即有輕度知能障礙(MCI),又稱失智前期(pre-dementia)。
● 明顯阿茲海默症:又依嚴重度可分為輕度(初期)、中度(中期)、重度(晚期)。
而開始發生認知功能障礙是在前驅期,通常被稱為輕度知能障礙(MCI),其特徵在於認知症狀的發作,如記憶或其他認知功能障礙,但尚未符合失智的標準。一般而言,輕度知能障礙在正常老化到失智症開始出現徵兆之間,存在著過渡期,此時雖未符合阿茲海默症診斷標準,但患者在面臨較複雜的工作或社會環境下會有問題;而簡易之日常生活並無影響,因此容易被忽略而延誤早期發現的時機。然而,目前醫學已能夠透過檢測「生物標記」的方式,檢驗出前驅期的阿茲海默症。
▎利用生物標記偵測阿茲海默症
當老年患者到醫院主訴記憶衰退時,第一步須先客觀確認是否真有認知功能受損。如果經由病史、床邊認知檢測或進一步的神經認知功能測試,仍無法客觀確認有無認知問題,則不建議進行下一步生物標記檢查。
若確定有認知功能受損時,第二步則是先區分是否為神經退化性疾病。如果病因不是神經退化性疾病,就有可能是可治癒的失智症。若確認是神經退化性,則需確認患者的神經退化性是否為阿茲海默症引起,以俾提出輔助性治療,以延緩失智症的進展。
失智症的確診,是基於臨床症狀及阿茲海默症患者類澱粉蛋白和tau蛋白(附註1)的病理學證據。阿茲海默症的生物標記可分二大類:
(一)偵測到腦澱粉樣病變(Amyloidosis)的存在。
(二)必須反映神經元受損的情形,即神經退化(Neurodegeneration)。對偵測早期阿茲海默患者最有助益和實用的生物標記就是檢測神經退化。以下是常用的三種生物標記:
(1) 阿茲海默症病理的tau蛋白CSF測試:只能對特定類型進行檢測(阿茲海默症),所以會遺漏其他類型的退化性失智症(如:路易士體失智症、額顳葉型失智症等),因為它無法廣泛檢出所有神經退化性原因,所以不適合做失智症的第一線篩檢工具。
(2) 氟化去氧葡萄糖正子造影(FDG-PET):理論上這種檢查可以提供神經退化信息,但到目前為止,FDG-PET僅被證明較適用於區分神經退化性疾病種類,而不是檢測是否存在神經退化。
(3) 磁振造影術(MRI):既可直接看到全腦構造(圖四),又可看見阿茲海默症易損部位,如:海馬迴的萎縮及皮質變薄等(圖五)。可同時提供較完整的信息,所以成為目前失智症最重要的篩檢與診斷工具。

(圖四)正常人的大腦(左)與阿茲海默症病患的大腦(右),標識處為相異的特徵│資料來源:維基百科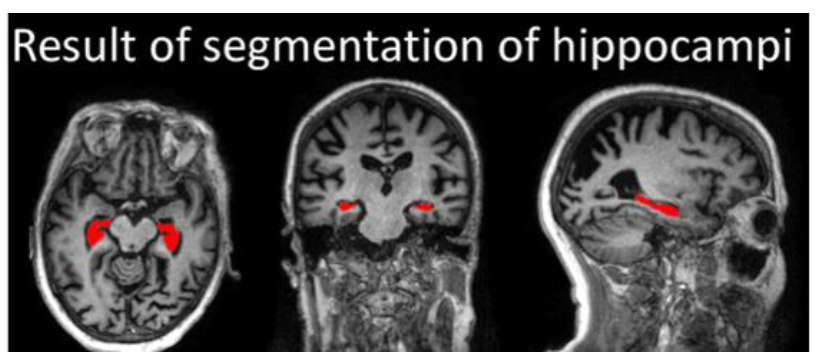
(圖五)腦部三種切面,紅色區域即為海馬迴位置。│ NeuroImage: Clinical 11 (2016) 435-49
▎透過不同的生物標記,可得知阿茲海默病程變化順序
由下方曲線可以看出腦澱粉樣病變(紅色)及tau蛋白(藍色)的異狀發生在先,接著腦部組織結構在MRI影像(黃色)產生變化,最後才是知能障礙(紫色)以及臨床功能障礙(綠色)。換句話說,患者在意識到認知障礙(臨床前期)產生之前,即可透過腦澱粉樣病變、tau蛋白升高及腦部組織結構在MRI影像的變化等生物標記做偵測。

▎磁振造影術在臨床應用的優勢
腦澱粉樣病變雖能最早偵測出阿茲海默症的可能性,但研究發現:約30%健康且認知正常的人也有澱粉樣病變,且陽性率會隨年齡而增加;80歲以上認知健康的老人,65%有類澱粉蛋白堆積增加的現象。而阿茲海默症的病程,可能在認知功能障礙症狀發生的前15至20年就開始了;長而多變的臨床前期病程,甚至終其一生也不一定會經歷失智症任何症狀。
研究發現,神經元損傷指標(如:MRI)所見的萎縮,要比類澱粉蛋白陽性,更能預測即將發生認知功能的衰退症狀;若只發現腦澱粉樣病變,沒有檢測神經退化,是無法預測即將的失智風險,而受檢者也可能徒增心理負擔,反而不利於健康。
根據研究指出,在阿茲海默症發病之前的臨床前期及前驅期,即會有廣泛性大腦萎縮,並且在腦部區域海馬迴有不等程度的萎縮(圖七),故可運用腦部影像來預測失智症。此外,CT和MRI可同時看到腦血管疾病的狀況,即小血管缺血病變的診斷;此時若發現腦部有較多白質斑塊產生,將會增加認知功能衰退的風險,其預後也較差。
此外,研究顯示,大約一半有內側顳葉萎縮的輕度知能障礙患者,約會在18個月內得到失智症;而超過80%的患者將在三年內失智。因此,有記憶障礙的患者,若被證實有內側顳葉萎縮,預測3年內會有很高風險發生失智症。
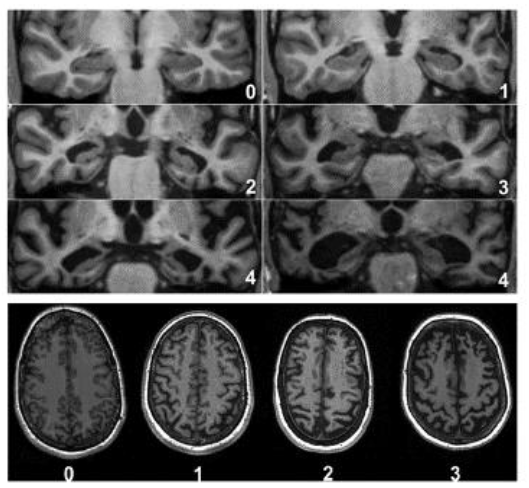
(圖七)內側顳葉萎縮和大腦皮質萎縮程度分級。│J Neurol Neurosurg Psychiatry. 2015 Nov;86(11):1225-33
▎阿茲海默症有可能被提前檢查出來嗎?
傳統上,CT和MRI影像檢測,是用於排除其他可能導致認知功能障礙疾病的工具;然而,在現代臨床檢查中,CT和MRI已成為失智症的檢測基石,因為他們能夠直接檢測神經退化性疾病具特異性(Specific)的腦萎縮形態,例如:偵測內側顳葉萎縮(阿茲海默症早期徵兆)。同時,MRI不具輻射線,對於腦部組織結構分析優於CT,故目前已被廣泛使用中。 早期發現早期治療或能有效延緩疾病的進行,這也是目前醫學界努力研究的方向。
註1. Tau蛋白(Tau proteins),又譯濤蛋白。是一種微管相關蛋白,tau蛋白有缺陷並不再正常穩定微管時,可導致神經系統病變和失智症,如阿茲海默病。│資料來源:維基百科